
Reportée d’un an en raison de la pandémie, la réglementation 2017/745 concernant les appareils classés « dispositifs médicaux » entre en vigueur le 26 mai 2021 : une véritable révolution qui concerne toute la filière esthétique ! Minceur, anti âge, dépilation : presque tous les appareils utilisés couramment par les instituts de beauté sont concernés. Quelles sont les nouvelles obligations pour les fabricants et les esthéticiennes ? Comment va s’appliquer le calendrier ? Va t-on enfin vers la fin des litiges entre ce qui ressort du secteur médical et du secteur esthétique ? Estheticienne.pro vous explique ce que la nouvelle réglementation européenne sur les appareils esthétiques va changer.
Sommaire
- Une mise sur le marché sans contraintes ni contrôles
- Ce que la nouvelle réglementation européenne sur les appareils esthétiques va changer
- Quels sont les appareils esthétiques concernés par la classification « DM » ?
- Les nouvelles obligations des fabricants d’appareils esthétiques classés « DM »
- Une procédure de certification complexe
- Des contrôles à venir dans les instituts
- A quoi sert le portail européen Eudamed ?
- Comment va s’appliquer le règlement européen 2017/745 ?
- Une clarification attendue
Une mise sur le marché sans contraintes ni contrôles
Quelle est la situation actuelle ? Jusqu’ici, la plupart des appareils esthétiques commercialisés auprès des instituts de beauté ne rentraient dans aucune catégorie particulière aux yeux de la loi. En clair, un appareil esthétique pouvait être importé et commercialisé en France sans plus de formalités qu’un sèche-cheveux ou un aspirateur, avec une simple conformité « CE électrique ». Cependant, certains fabricants avaient déjà entrepris d’obtenir un certificat CE Médical. Celui-ci va être renforcé et actualisé au titre de la nouvelle réglementation Européenne.
Ce que la nouvelle réglementation européenne sur les appareils esthétiques va changer
La majorité des appareils high tech distribués aux instituts de beauté sont aujourd’hui dérivés de technologies médicales, confrontant les esthéticiennes aux mêmes risques d’utilisation que les médecins. Constatant cette convergence, les autorités sanitaires ont élargi la notion de « dispositif médical » (DM) à des matériels n’ayant aucune finalité en matière de soin ou de diagnostic. Autrement dit, un appareil peut désormais être classé « DM » alors qu’il n’est pas utilisé par des médecins et n’a aucun rapport avec la santé.
Les dispositifs médicaux entrent dans un cadre réglementaire contraignant, comprenant une procédure de mise sur le marché, puis des obligations de surveillance et de traçabilité.
En incluant la plupart des appareils esthétiques dans la liste des dispositifs médicaux, le législateur souhaite imposer des standards harmonisés de qualité, de sécurité et de fiabilité à tous les matériels esthétiques distribués sur le marché Européen. L’objectif ? Réduire les accidents potentiels en instituts de beauté et sécuriser le consommateur final.
Quels sont les appareils esthétiques concernés par la classification « DM » ?
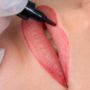
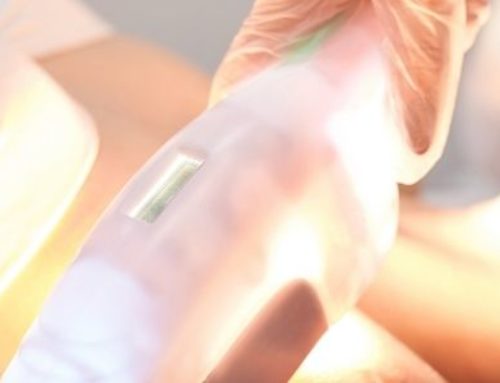
La première liste dressée dans l’annexe XVI du règlement 2017/745 englobe déjà la plupart des technologies esthétiques en matière d’anti âge et minceur : infrarouges, leds, ultrasons, dermabrasion, radiofréquence, cryo-esthétique, lipocavitation. Sont également concernés les solariums (émission d’UV). Et, bien sûr, les appareils de dépilation (lumière pulsée et lasers).
Vouée à évoluer, cette liste n’est pas exhaustive. On sait d’ores et déjà qu’elle intègrera automatiquement toute technologie « destinées à effectuer un comblement pour la peau par voie sous cutanée ou tout autre mode d’introduction », tout équipement destiné « à réduire, enlever ou détruire des tissus adipeux » ou « émettant des rayonnements à haute intensité », sans compter « d’autres traitements cutanés » à définir…
La liste pourrait donc être longue.
Les nouvelles obligations des fabricants d’appareils esthétiques classés « DM »
A partir du 26 mai 2021, les fabricants et importateurs qui distribuent des appareils esthétiques sous leur propre marque seront soumis à trois obligations principales avant commercialisation :
- faire certifier leurs appareils classés « DM » par un organisme agréé (ON)
- définir un contenu de formation obligatoire pour utiliser leurs appareils
- s’enregistrer sur le portail européen Eudamed
Après certification, le fabricant devra également suivre tous les incidents remontés par les instituts dépositaires et concevoir des mesures correctives en matière de fabrication ou de formation.
Des contrôles réguliers effectués par les organismes de certification vérifieront que les fabricants respectent bien ces obligations dans le temps.
Une procédure de certification complexe
Valable cinq ans, la certification d’un appareil esthétique n’est pas une simple formalité – loin de là.
Pour obtenir le précieux sésame, les fabricants doivent respecter de nombreuses exigences en matière de conception et de fabrication. Il leur est demandé de produire un rapport d’évaluation des risques d’utilisation de leur appareil. Ils doivent également se soumettre à un audit externe. Mais surtout, ils ont pour la première fois l’obligation d’effectuer une étude clinique sur un échantillon de consommateurs, de manière à mesurer scientifiquement l’efficacité et l’innocuité de leurs appareils.
Cette procédure, longue, complexe et coûteuse, effraie (à raison) de nombreux acteurs du marché. La pandémie a retardé la diffusion de l’information. Les interlocuteurs pour expliquer les textes manquent. Les contours exacts de la nouvelle réglementation, la liste exhaustive des DM concernés et l’agrément des organismes de certification arrivent au compte-gouttes. Un vent de panique souffle donc sur la filière esthétique, d’autant que seuls treize organismes sont actuellement aptes à délivrer la certification pour toute l’Europe, faisant craindre un embouteillage au niveau des dossiers.
Des contrôles à venir dans les instituts
Si la plupart des contraintes imposées par la nouvelle réglementation sont destinées aux fabricants, il appartient désormais aussi aux esthéticiennes de s’équiper d’appareils bénéficiant d’un certificat conformité. Il est d’ailleurs probable que des contrôles soient menés d’ici quelques mois par l’ANSM dans les instituts de beauté – à l’instar de ce qui se pratique pour les appareils à UV (qui sont d’ailleurs concernés !).
Autre conséquence de la nouvelle réglementation : acheter (en ligne) un appareil esthétique provenant d’un pays extérieur à l’Union Européenne devient extrêmement risqué : en cas de contrôle, l’esthéticienne sera de fait considérée comme « importateur » et passible d’une amende conséquente – en plus de voir l’appareil saisi. Il en va d’ailleurs de même pour les distributeurs, qui sont responsables de la mise sur le marché.
Comment savoir si un appareil esthétique est conforme au règlement européen ? Dans les deux ans, tous les « DM » devront faire l’objet d’un marquage « CE médical » qui comprendra un numéro unique d’identification (IUD) délivré par l’organisme de certification. Par ailleurs, dans un souci de transparence, la base Eudamed sera accessible au public en 2022 pour vérification. En attendant, l’institut peut exiger de son fournisseur un certificat de conformité qui pourra être présenté en cas de contrôle.
Les appareils achetés avant le 26 mai 2021 ne sont pas concernés.
A quoi sert le portail européen Eudamed ?
Lancé en décembre 2020, le portail Eudamed devient le répertoire de tous les dispositifs médicaux certifiés pouvant être commercialisés en Europe. Tout fabricant (ou importateur diffusant sous sa propre marque dans l’Union) doit s’y enregistrer en tant qu’opérateur économique puis y déclarer les appareils esthétiques classés DM qu’il distribue sous un numéro unique d’identification (IUD).
Mais Eudamed n’est pas simplement un portail d’enregistrement pour les fournisseurs. Sa vocation est également d’informer le public. Les autorités ont par exemple décidé de publier certaines données sensibles comme les résultats des tests cliniques menés par les marques. A partir de 2022, sa base de données deviendra en grande partie accessible aux esthéticiennes, qui pourront ainsi vérifier les allégations des fournisseurs avant de s’équiper.
Comment va s’appliquer le règlement européen 2017/745 ?
Le calendrier du nouveau règlement européen sur les dispositifs médicaux va se mettre en place par étapes.
Pour tout appareil lancé sur le marché, le nouveau règlement européen s’applique immédiatement : à partir du 26 mai 2021, aucun nouveau produit ne pourra être commercialisé sans un certificat de conformité valide et un numéro unique d’identification (IUD), qui sera à enregistrer dans Eudamed dans les 18 mois après sa mise sur le marché.
En revanche, les appareils qui étaient déjà commercialisés sous la nomenclature « DM » avant le 26 mai 2021 disposeront d’une période de grâce de 3 ans pour se mettre en conformité avec le nouveau règlement européen. Autrement dit, jusqu’en mai 2024, ces appareils pourront encore être produits et commercialisés – sous réserve d’appliquer certaines dispositions (surveillance après commercialisation et enregistrement dans Eudamed). Attention : cette tolérance ne concerne que les fournisseurs qui distribuent des appareils déjà marqués « CE médical » ou bénéficient d’un certificat valide au titre des précédentes directives (93/42/CE ou 90/385/CE).
A partir du 26 mai 2024, les anciens certificats « directives » ne seront plus valables. Les distributeurs pourront encore commercialiser les appareils en stock durant un an (mais il ne sera plus possible d’en fabriquer).
Le 26 mai 2025, tous les appareils esthétiques classés DM devront être conformes au nouveau règlement Européen. Les appareils sans certificat ne pourront plus être commercialisés.
Par conséquent, entre 2021 et 2025, les esthéticiennes pourront acquérir des appareils ayant un certificat « directive » ou un certificat « règlement Européen 2017/745 ». Quel que soit le cas, elles seront couvertes en cas de contrôle.
Concernant l’étiquetage obligatoire sur les appareils, un délai de deux ans à partir de mai 2021 est laissé aux fabricants pour apposer le CE Médical avec le numéro IUD. Cette dérogation de calendrier n’est pas valable pour les dispositifs de classe III.
Une clarification attendue
Pouvait-on interdire les technologies du vingt et unième siècle aux esthéticiennes ? L’histoire a montré que non. Le progrès finit toujours par s’imposer, y compris en France, qui a pourtant vu se multiplier les procès pour exercice illégal de la médecine – du palper rouler à la lumière pulsée. Cette question a soulevé beaucoup moins de débats chez nos voisins, plus libéraux. Finalement, les autorités sanitaires Européennes ont tranché : en harmonisant la réglementation dans toute l’Union, le nouveau règlement 2017/745, s’il impose de nouvelles contraintes, préserve aussi les distributeurs comme les esthéticiennes des recours intentés par le puissant lobby médical. Une excellente nouvelle pour la filière esthétique française, qui vivait dans le flou le plus total depuis une vingtaine d’années, laissant aux tribunaux le soin d’arbitrer les controverses.
L’insécurité juridique constitue un frein puissant au développement. Qu’on soit à la tête d’un institut ou distributeur, comment investir sereinement en ayant constamment une épée de Damoclès au dessus de la tête ? Si l’entrée en vigueur du nouveau règlement Européen constitue un défi à surmonter dans les prochains mois, celui-ci clarifie aussi implicitement le droit du secteur esthétique de profiter des dernières technologies dans les domaines de la minceur, de l’anti âge et de la dépilation, ouvrant une nouvelle étape vers la transformation nécessaire de la profession.
Certes, cette mise en conformité a un coût, et son entrée en vigueur à la sortie de la crise sanitaire tombe mal. Il est même probable que la nouvelle réglementation écarte certains fournisseurs – ou en décourage d’autres d’entrer sur le marché. D’un autre côté, elle facilitera aussi la libre circulation en Europe des produits agréés. En effet, la loi Européenne va s’appliquer dans tous les pays de l’Union de la même façon et au même moment. Les fabricants souhaitant commercialiser en Europe n’auront donc plus désormais qu’un interlocuteur (l’ON) et seront dispensés de toute obligation d’enregistrement auprès des autorités sanitaires de chaque pays. Une forme de simplification, en somme.
Abonnez-vous gratuitement à la newsletter estheticienne.pro
L'information professionnelle décryptée chaque semaine.










J’ai lu et relu le fameux décret Européen mais je comprends que cela ne concerne que les importateurs (ou revendeurs) de machines hors CEE revendues avec une marque propre. Ce qui voudrait dire qu’il serait toujours possible d’acheter une machine hors CEE pour autant qu’on ne la revente pas (donc pour un usage privé ou professionnel)
Quasiment tous les lasers sont fabriqués et assemblés en Chine, avec des composants allemands, italiens, japonais…
Je connais au moins 4 « grandes marques » sur les marchés du benelux, Espagne et France qui prétendent fabriquer leur laser sous leur marque. En fait les machines sont fabriquées réellement en Chine avec une carcasse sur mesure. Un laser dépilatoire serait selon ma compréhension obligé d’avoir l’agrément CE mais pas CE médical…. ? .
En, effet, si on lit le décret ont peut voir:
ANNEXE XVI LISTE DES GROUPES DE PRODUITS N’AYANT PAS DE DESTINATION MÉDICALE PRÉVUE VISÉS À L’ARTICLE 1ER, PARAGRAPHE 2
L’ARTICLE 1ER, PARAGRAPHE 2 : «accessoire de dispositif médical», tout article qui, sans être lui-même un dispositif médical, est destiné par son fabricant à être utilisé avec un ou plusieurs dispositifs médicaux donnés pour permettre une utilisation de ce ou ces derniers conforme à sa ou leur destination ou pour contribuer spécifiquement et directement à la fonction médicale du ou des dispositifs médicaux selon sa ou leur destination;
ANNEXE XVI LISTE DES GROUPES DE PRODUITS N’AYANT PAS DE DESTINATION MÉDICALE PRÉVUE VISÉS À L’ARTICLE 1ER, PARAGRAPHE 2 :
5. Équipements émettant des rayonnements électromagnétiques à haute intensité (infrarouge, lumière visible, ultraviolet par exemple) et destinés à être utilisés sur le corps humain, y compris les sources cohérentes et non cohérentes, monochromes et à large spectre, tels que les lasers et les équipements à lumière intense pulsée utilisés pour le resurfaçage cutané, la suppression de tatouages, l’épilation ou d’autres traitements cutanés.
Bonjour,
Voici ce que dit l’article 1 er : « Le présent règlement s’applique également (…) aux groupes de produits n’ayant pas de destination médicale, dont la liste figure à l’annexe XVI.
Les produits listés dans l’annexe 16 sont donc bien ceux qui tombent sous le règlement (et non pas ceux qui y échappent !). Et parmi ceux ci, on trouve de façon très claire : « les lasers et les équipements à lumière intense pulsée ».
Il n’y a aucune ambiguïté permettant une interprétation. L’ANSES vient d’ailleurs de le rappeler dans un communiqué jeudi 9 septembre 2021.
Je pense que le titre de l’annexe 16 est mal formulé, d’où votre confusion (en gras ci-dessous les deux mots de liaison qui aideraient à comprendre).
LISTE DES GROUPES DE PRODUITS N’AYANT PAS DE DESTINATION MÉDICALE PRÉVUE QUI SONT VISÉS À L’ARTICLE 1ER, PARAGRAPHE 2 (en clair : liste des dispositifs non médicaux mais tout de même astreint au nouveau règlement).